dostarlimab está disponível na Bélgica (e o que fazer entretanto)?
Última atualização: 15 de janeiro de 2024

Pode aceder legalmente a novos medicamentos, mesmo que estes não estejam aprovados no seu país.
Saiba comoDostarlimab (comercialmente vendido como Jemperli) é uma nova terapia anti-PD-1. Recebeu autorização condicional de comercialização da EMA em 2021 para o tratamento do cancro endometrial avançado ou recorrente [1]. Com isso, tornou-se a primeira terapia anti-PD-1 aprovada na Europa para esta indicação.
Para os doentes com tumores deficientes em reparação de incompatibilidades (dMMR), este é um grande marco. Especialmente porque a inovação neste domínio tem ficado para trás, de acordo com Jack Harris, Vice-Presidente da GSK para a Oncologia no Reino Unido [2].
No entanto, as pessoas ansiosas por iniciar o tratamento com dostarlimab na Bélgica podem precisar de um pouco mais de paciência. Pode ainda demorar algum tempo até que o medicamento esteja amplamente disponível no mercado.
dostarlimab está disponível na Bélgica?
Atualmente, dostarlimab não está amplamente disponível no mercado belga.
Após a sua autorização condicional de introdução no mercado em 2021, dostarlimab tem estado disponível na Bélgica como parte de dois programas de uso compassivo:
- Um deles centrou-se no dostarlimab como agente único no tratamento do cancro do endométrio dMMR/MSI-H recorrente ou avançado que tenha progredido após tratamento prévio. Este programa foi encerrado em 2022 [3].
- Um deles centrou-se no dostarlimab em combinação com quimioterapia como tratamento de primeira linha do cancro do endométrio primário avançado ou recorrente dMMR/MSI-H. Este programa ainda está ativo [3].
Dostarlimab também tem outra indicação aprovada pela FDA, para utilização no tratamento de tumores sólidos avançados ou recorrentes dMMR/MSI-H. Para esta indicação, não está atualmente aprovado pela EMA e não está disponível na Bélgica.
Quando é que dostarlimab estará disponível na Bélgica?
A obtenção da autorização total de introdução no mercado da EMA (prevista para 2024) será o primeiro passo para a disponibilização dostarlimab no mercado belga. Se for aprovado pelo FAMHP para inclusão na via de tratamento, terão também de ser tomadas decisões sobre os preços locais e a cobertura dos seguros de saúde.
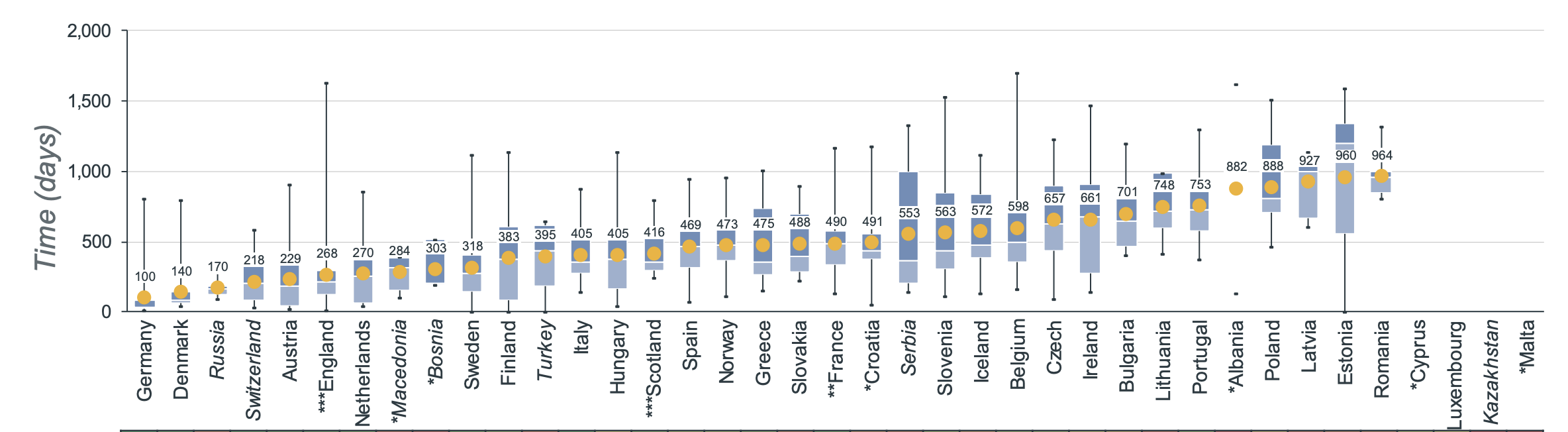
O tempo médio necessário desde o momento em que um medicamento obtém a aprovação da EMA até ao momento em que está disponível no mercado varia muito consoante o país. A média europeia para os tratamentos oncológicos em 2022 foi de 511 dias entre a autorização de introdução no mercado da EMA e a data de ampla disponibilidade. Na Bélgica, o tempo médio até à disponibilidade é de 598 dias [4].
Neste contexto, poderá ainda demorar algum tempo até que dostarlimab esteja amplamente disponível no mercado belga.

O que pode fazer até o dostarlimab chegar à Bélgica?
É uma doente na Bélgica com cancro do endométrio, que não é elegível para o programa de uso compassivo? Ou é um doente com um tumor sólido dMMR/MSI-H avançado? Se o seu médico recomendar o tratamento com dostarlimab, tem opções.
Quando um medicamento não está aprovado no país de um doente, ou está aprovado mas ainda não está disponível, pode aceder-lhe através do regulamento de Importação de Doentes Nomeados.
Everyone.org é especializada em ajudar as pessoas a aceder aos medicamentos mais recentes através deste regulamento. Se tem uma receita do seu médico assistente para o Jemperli dostarlimab), está impaciente por iniciar o seu plano de tratamento e gostaria que o ajudássemos a ter acesso imediato ao medicamento, contacte-nos.
Referências:
- Jemperli | Agência Europeia de Medicamentos. Agência Europeia de Medicamentos, 21 de abril de 2021.
- Cooper, Emma. Pacientes do Reino Unido têm acesso antecipado ao tratamento da GSK para o cancro do endométrio. Pf Media, 10 de julho de 2023.
- Uso compassivo - Necessidade médica. FAMHP, Acedido em 25 de setembro de 2023.
- Inquérito de 2021 sobre o indicador W.A.I.T. dos doentes da EFPIA. EFPIA, Acedido em 25 de setembro de 2023.