Quando é que a Vamorolone estará disponível na Europa e no Reino Unido? A história completa.
Última atualização: 16 de abril de 2024

Pode aceder legalmente a novos medicamentos, mesmo que estes não estejam aprovados no seu país.
Saiba comoOs corticosteróides têm sido um tratamento padrão para os doentes com Distrofia Muscular de Duchenne durante muitos anos. Normalmente, são incluídos no plano de tratamento por volta dos 4 ou 5 anos de idade, antes de entrarem na "fase de planalto" e sofrerem uma perda significativa de força 1. Infelizmente, a utilização prolongada de corticosteróides pode estar associada a vários efeitos secundários, incluindo problemas de comportamento, aumento de peso, osteoporose, entre outros 2.
Neste contexto, a recente aprovação pela FDA do Agamree (vamorolona) como um "corticosteroide da nova vaga" com menos efeitos secundários foi um avanço muito necessário no tratamento de Duchenne.
Embora a vamorolona já seja esperada nas farmácias dos EUA no primeiro trimestre de 2024, ainda não foi aprovada em mais nenhum lugar.
Quando é que a vamorolona estará disponível na Europa e no Reino Unido? Aqui está tudo o que precisa de saber.
Para que é utilizada a vamorolona?
Agamree (vamorolona) é indicado para o tratamento de crianças (4+) e adultos com distrofia muscular de Duchenne.
O Agamree é um corticosteroide dissociativo. A sua ação consiste principalmente em acalmar a inflamação no organismo. A vamorolona actua de forma semelhante a outros corticosteróides. No entanto, liga-se às células de forma diferente e não ativa certas respostas do corpo como fazem os outros esteróides.
Não se compreende completamente como é que o vamolorone actua na DMD (Distrofia Muscular de Duchenne). No entanto, os resultados dos ensaios clínicos sugerem que ajuda as crianças com esta doença a levantarem-se mais rapidamente e a caminharem melhor. Alguns dos efeitos secundários habituais incluem o aparecimento de inchaço, vómitos, aumento de peso e irritação 3.
A vamorolona foi aprovada pela EMA?
Desde dezembro de 2023, o Agamree (vamorolona) foi aprovado pela EMA para o tratamento da distrofia muscular de Duchenne em adultos e crianças com mais de 4 anos de idade. 3.
Quando é que a vamorolona estará disponível na Europa?
Embora a aprovação da vamorolona pela EMA seja uma boa notícia, não significa que o medicamento estará disponível de imediato em todos os países europeus. Antes de chegar às farmácias, o fabricante do medicamento e as autoridades de saúde locais de cada Estado-Membro têm de tomar decisões sobre a aprovação local, os preços e a cobertura dos seguros de saúde. Como resultado, a vamorolona estará provavelmente disponível em alturas diferentes em cada país da Europa.
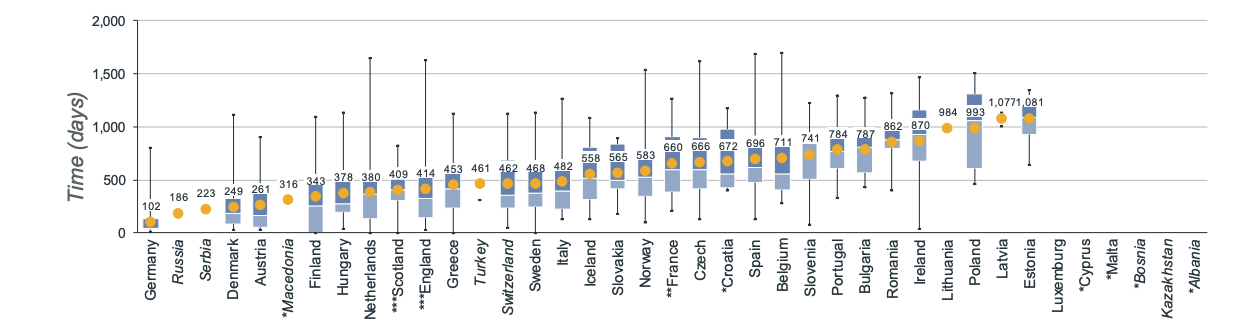
Os novos medicamentos demoram, em média, 511 dias após a aprovação da EMA para estarem disponíveis em toda a UE. Este prazo é muito diferente consoante o país. No caso dos medicamentos órfãos, como a vamorolona, varia entre 102 dias na Alemanha e 1 081 dias na Estónia 5.
Quando é que a vamorolona estará disponível no Reino Unido?
Após a aprovação da EMA, a vamorolina é agora também aprovada pela MHRA no Reino Unido. Isto faz com que o medicamento seja o primeiro tratamento de Duchenne a ser aprovado no Reino Unido, na UE e nos EUA coletivamente.
Antes de a vamorolona estar disponível no NHS, o NICE tem de rever e publicar a sua decisão sobre o assunto. As consultas estão em curso e espera-se um projeto de orientação até ao final de abril de 2024 6 . Em caso afirmativo, o Agamree deverá estar disponível para os doentes no prazo de 3 meses a contar da data da decisão do NICE.
Estado de aprovação da vamorolona no resto do mundo
A partir de abril de 2024, o Agamree (vamorolona) não está aprovado em mais nenhum lugar do mundo para o tratamento da distrofia muscular de Duchenne 7.

Formas de acesso seguro ao Agamree (vamorolone) antes de ser aprovado no seu país
É um doente de Duchenne fora dos EUA? Se o seu médico acha que a vamorolona o pode ajudar, talvez não tenha de esperar pela aprovação ou disponibilidade local do Agamree. Em vez disso, o seu médico e você podem explorar os ensaios clínicos da vamorolona. Ou, pode comprar vamorolona imediatamente como um Paciente Individual Nomeado.
Participar num ensaio clínico com vamorolone
Pode participar num ensaio clínico para obter Agamree (vamorolona) ou outros medicamentos não aprovados. Encontrar um ensaio que esteja a recrutar participantes no seu país pode ser difícil, mas é possível. Para participar no ensaio, tem de cumprir os critérios de elegibilidade. Necessitará também do apoio do seu médico assistente.
Aqui estão alguns bons sítios para começar a procurar ensaios clínicos de vamorolone em curso:
- ClinicalTrials.gov: Esta é uma base de dados com todos os ensaios clínicos nos EUA. Alguns dos ensaios também estão abertos a participantes internacionais. Um exemplo é o ensaio clínico NCT05185622 com vamorolona, que está a recrutar doentes no Canadá 8.
- EUClinicaltrials.eu: Esta base de dados contém todos os ensaios clínicos na União Europeia. Atualmente, contém informações limitadas sobre ensaios lançados antes de 31 de janeiro de 2022. Para esses ensaios, pode consultar o Registo de Ensaios Clínicos da UE.
- myTomorrows: Esta organização apoia os doentes na procura de opções de tratamento em ensaios clínicos.
Comprar vamorolone numa base de doente individual nomeado
Na maioria dos países, os doentes estão legalmente autorizados a comprar e importar medicamentos que possam melhorar a sua vida ou tratar doenças potencialmente fatais. Se quiser ter acesso à vamorolona antes de estar disponível no seu país, esta pode ser uma opção para si e para o seu médico.
O regulamento que torna isto possível é conhecido como o regulamento relativo à importação de doentes individuais designados. Pode haver variações entre os países em termos de requisitos administrativos específicos. No entanto, em todos os casos, estes critérios devem ser cumpridos:
-
O medicamento em questão tem aprovação de mercado noutro país e não está (ainda) aprovado ou disponível no país do doente;
-
Não existe qualquer alternativa no mercado local;
-
O medicamento é para uso pessoal;
-
O paciente tem uma carta de prescrição do seu médico assistente;
-
O médico assume a responsabilidade pelo tratamento. Este facto pode exigir documentação diferente de país para país.
Pretende utilizar o regulamento relativo à importação de doentes individuais designados para obter vamorolona antes de esta estar amplamente disponível na Europa, no Reino Unido ou noutro local? Em primeiro lugar, terá de consultar o seu médico assistente e obter uma receita médica adequada.
Já tem uma receita médica? A nossa equipa pode ajudá-lo a comprar vamorolone imediatamente.
Referências:
- Esteróides (corticosteróides). Parent Project Muscular Dystrophy, Acedido em 13 de novembro de 2023.
- Side Effects of Long Term High-Dose Steroid Therapy, Acedido em 13 de novembro de 2023.
- Agamree: Autorizado | Agência Europeia de Medicamentos. Agência Europeia de Medicamentos, 13 de outubro de 2023.
- Pedido de autorização de introdução no mercado na UE de medicamentos para uso humano. Agência Europeia de Medicamentos, Acedido em 13 de novembro de 2023.
- Inquérito EFPIA Patients W.A.I.T. Indicator 2021. Efpia, Acedido em 13 de novembro de 2023.
- Informação sobre o projeto | Vamorolone for treating Duchenne muscular dystrophy [ID4024] | Guidance. NICE, Acedido em 13 de novembro de 2023.
- AGAMREE® (vamorolona) - santhera. Santhera, Acedido em 13 de novembro de 2023.
- A Study to Assess Vamorolone in Boys Ages 2 to <4 Years and 7 to <18 Years With Duchenne Muscular Dystrophy (DMD). ClinicalTrials.gov, Accessed 13 November 2023.