Adakveo vs Oxbryta: Conhecer as alternativas crizanlizumab
Última atualização: 15 de janeiro de 2024
Pode aceder legalmente a novos medicamentos, mesmo que estes não estejam aprovados no seu país.
Saiba como
Na sequência da revogação da autorização do Adakveo crizanlizumab) na UE, muitos doentes e médicos precisam de encontrar uma alternativa Adakveo .
Se tiver respondido bem ao tratamento, pode continuar a ter acesso ao Adakveo , mesmo que este já não esteja aprovado na UE. No entanto, se o seu médico preferir alterar o seu tratamento, é bom compreender o que isso significa para si enquanto doente.
Neste artigo, vamos analisar uma das possíveis alternativas Adakveo que o seu médico poderá querer discutir - Oxbryta voxelotor). Aqui encontrará uma breve descrição geral das semelhanças e diferenças entre Adakveo e Oxbryta.
Adakveo vs Oxbryta: Para que é que são utilizados?
Tanto Adakveo como Oxbryta são medicamentos sujeitos a receita médica indicados para o tratamento da doença falciforme 1,2. Cada um dos medicamentos, no entanto, tem como objetivo um aspeto diferente da doença.
Adakveo tem como objetivo reduzir a frequência das crises vaso-oclusivas dolorosas, enquanto Oxbryta é utilizado para tratar a anemia hemolítica em doentes com células falciformes 1,2.
Para que idade é que Oxbryta está aprovado na UE?
Ao contrário do Adakveo, que só pode ser utilizado em doentes com idade igual ou superior a 16 anos, Oxbryta está também indicado para doentes pediátricos.
Nos EUA, Oxbryta pode ser prescrito a partir dos 4 anos de idade, enquanto na UE, a utilização pediátrica só é aprovada a partir dos 12 anos 1,2.
Crizanlizumab vs Voxelotor: Como é que funcionam?
Embora ambos os medicamentos tenham como objetivo reduzir as complicações da doença falciforme, visam aspectos diferentes da doença.
Adakveo e a redução das crises dolorosas
O objetivo Adakveo é reduzir a frequência das crises dolorosas, que ocorrem quando as células sanguíneas malformadas ficam presas nos vasos sanguíneos.
A substância ativa do medicamento, o crizanlizumab, é um tipo específico de proteína conhecido como anticorpo monoclonal. Esta proteína está formulada para se ligar à P-selectina, uma substância que se encontra na camada exterior das células que revestem os vasos sanguíneos.
A P-selectina ajuda as células a aderirem aos vasos sanguíneos e está envolvida no bloqueio dos vasos durante os episódios dolorosos da doença falciforme. Ao ligar-se à P-selectina e inibir a sua função, Adakveo pretende prevenir estes episódios dolorosos 3.
Oxbryta e a prevenção da anemia
Oxbryta, por outro lado, tem como objetivo prevenir a anemia associada à doença falciforme.
A substância ativa do Oxbryta, o voxelotor, aumenta a capacidade da hemoglobina para reter o oxigénio e impede-a de formar cadeias rígidas no interior dos vasos sanguíneos. Isto ajuda os glóbulos vermelhos a manter a sua forma e flexibilidade normais. Reduz também a taxa da sua destruição prematura e prolonga a sua vida 4.
Qual a eficácia do Adakveo e Oxbryta?
A eficácia do Adakveo crizanlizumab) e do Oxbryta voxelotor) foi estudada em ensaios clínicos.
-
Resultados dos ensaios clínicos Adakveo
A aprovação do Adakveo pela FDA, bem como a sua autorização inicial de comercialização na UE, basearam-se nos resultados do estudo clínico SUSTAIN. O estudo comparou Adakveo (com ou sem hidroxiureia) com um placebo.
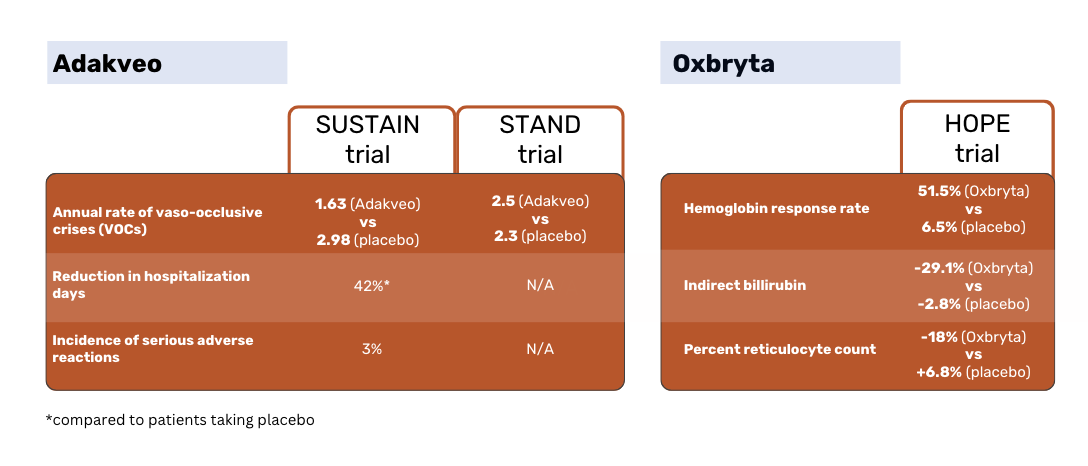
De acordo com os resultados do estudo SUSTAIN, os doentes tratados com Adakveo apresentaram uma taxa mediana anual de crises vaso-oclusivas (COV) estatisticamente significativa mais baixa - 1,63 contra 2,98 nos doentes que receberam placebo. 36% dos doentes tratados Adakveo no ensaio não tiveram COVs durante o período de 52 semanas do ensaio, em comparação com 17% dos doentes tratados com placebo 1.
Quais foram os resultados do ensaio Adakveo STAND?
O estudo STAND global de fase 3, que comparou novamente Adakveo com o placebo, não conseguiu demonstrar uma diferença estatisticamente significativa na taxa de COVs entre os grupos de doentes. Os doentes tratados com Adakveo tiveram em média 2,5 crises dolorosas num ano de tratamento - não significativamente diferentes das 2,3 crises em média registadas no grupo do placebo 3.
Os resultados pouco convincentes do ensaio STAND constituíram a base para a revogação daAdakveo na UE.
-
Resultados dos ensaios clínicos Oxbryta
No ensaio HOPE, Oxbryta foi testado contra um placebo. A eficácia baseou-se nas taxas de resposta de hemoglobina (Hb) definidas como um aumento de Hb de >1 g/dL desde a linha de base até à Semana 24.
Os doentes com Oxbryta tiveram uma taxa de resposta de 51,1% contra 6,5% dos doentes com placebo. A bilirrubina indireta diminuiu 29,1% nos doentes com Oxbryta , em comparação com uma diminuição de 2,8% nos doentes com placebo. A contagem percentual de reticulócitos diminuiu 18% nos doentes com Oxbryta e aumentou 6,8& nos doentes com placebo 2.
Como mostram os dados partilhados, não é possível fazer uma comparação direta entre os dois medicamentos, uma vez que foram utilizados critérios de eficácia diferentes nos respectivos ensaios clínicos. Uma vez que ambos os tratamentos abordam a doença falciforme de uma forma diferente, é provável que Oxbryta não seja um substituto direto do Adakveo, mas sim uma parte de um novo plano de tratamento que o seu médico elaborará para si.

Adakveo vs Oxbryta: Segurança e efeitos secundários
De acordo com a sua informação de prescrição, estes são os efeitos secundários mais comuns do Adakveo e Oxbryta:
Efeitos secundários Adakveo
- Náuseas
- Dores nas articulações
- Dores de costas
- Dores de estômago
- Febre1.
Durante o ensaio SUSTAIN, 3% dos doentes sofreram reacções relacionadas com a perfusão, caracterizadas por sintomas como dores de cabeça, arrepios, vómitos, diarreia, falta de ar ou pieira 1.
Efeitos secundários Oxbryta
- Dor de cabeça
- Diarreia
- Dores de estômago
- Náuseas
- Erupção cutânea
- Febre 2.
Menos de 1% dos doentes dos ensaios clínicos apresentaram reacções de hipersensibilidade graves, incluindo erupção cutânea, ligeira falta de ar, ligeiro inchaço facial e eosinofilia (aumento do número de glóbulos brancos)2.
Adakveo vs Oxbryta: Comparação de preços
Quando se trata de preços de medicamentos que ainda não foram aprovados ou não estão disponíveis, estes devem ser considerados meramente indicativos. O preço final pode variar consoante a sua localização ou o fornecedor.
Custos Adakveo por ano
A dose recomendada para o Adakveo é de 5 mg/kg de massa corporal de 4 em 4 semanas. Isto significa 13 perfusões por ano. Para uma pessoa que pesa 60 kg, seriam necessárias 13 perfusões x 300 mg de Adakveo, ou seja, 39 frascos para injetáveis do medicamento.
A um preço de cerca de 5 214 euros por frasco de 100 mg, o custo anual de um tratamento Adakveo ascende a cerca de 203 346 euros 5.
Custos Oxbryta por ano
A dose recomendada de Oxbryta para doentes com peso corporal superior a 40 kg é de 1500 mg de Oxbryta uma vez por dia, equivalente a 3 comprimidos de 500 mg cada.
Uma embalagem de 90 comprimidos de 500 mg custa cerca de 40,365 euros e é suficiente para um mês, com base na dosagem recomendada acima. Por conseguinte, o custo anual do tratamento Oxbryta ascende a 484 380 EUR 6.
Onde são aprovados Adakveo e Oxbryta ?
Adakveo crizanlizumab) está atualmente aprovado em vários países, incluindo os EUA, Canadá e Austrália 7,9,10. A sua autorização condicional de comercialização na UE foi revogada em maio de 2023 3.
Oxbryta voxelotor) está aprovado nos EUA, na UE e no Canadá 4,8,9. No entanto, na UE, Oxbryta ainda não está amplamente disponível no mercado, uma vez que o tempo entre a autorização e o lançamento no mercado pode variar significativamente consoante o país.
Adakveo ou Oxbryta não estão (já) aprovados ou disponíveis no seu país? Se você e o seu médico são da opinião de que estes tratamentos podem beneficiá-lo, entre em contacto com a nossa equipa de especialistas em Acesso aos Medicamentos. Podemos fornecer-lhe um orçamento personalizado para obter o medicamento para si.
Referências:
- DESTAQUES DA INFORMAÇÃO DE PRESCRIÇÃO. Novartis, Acedido em 27 de setembro de 2023.
- DESTAQUES DA INFORMAÇÃO DE PRESCRIÇÃO. Oxbryta, Acedido em 27 de setembro de 2023.
- Adakveo | Agência Europeia de Medicamentos. Agência Europeia de Medicamentos, Acedido em 27 de setembro de 2023.
- Oxbryta | Agência Europeia de Medicamentos. Agência Europeia de Medicamentos, Acedido em 27 de setembro de 2023.
- Comprar Adakveo (crizanlizumab) online. Everyone.org, Acedido em 27 de setembro de 2023.
- Comprar Oxbryta (voxelotor) online. Everyone.org, Acedido em 27 de setembro de 2023.
- Adakveo. Therapeutic Goods Administration (TGA), Acedido em 27 de setembro de 2023.
- A FDA aprova um medicamento para tratar a doença falciforme em pacientes pediátricos. FDA, 17 de dezembro de 2021.
- Novos medicamentos aprovados em 2019 - Meds Entry Watch. Canada.ca, 10 de fevereiro de 2021.
- A FDA aprova a primeira terapia direcionada para o tratamento de doentes com complicações dolorosas da doença falciforme. FDA, 15 de novembro de 2019.