O Enhertu pode tratar o cancro do ovário? Todos os dados, nada de exageros.
Última atualização: 15 de julho de 2024
Pode aceder legalmente a novos medicamentos, mesmo que estes não estejam aprovados no seu país.
Saiba comoEnhertu (fam-trastuzumab deruxtecan-nxki) foi aprovado pela primeira vez pela FDA em 2019 1. Nessa altura, foi indicado para o tratamento do cancro da mama HER2-positivo. Desde então, Enhertu tem sido aprovado para mais indicações. Estas incluem câncer gástrico HER2-positivo, câncer de mama HER2-baixo e câncer de pulmão HER2-mutante de células não pequenas. Desde abril de 2024, o tratamento está também aprovado pela FDA para utilização em todos os tumores HER2-positivos5.
Neste contexto, o sítio Enhertu tem atraído muita atenção dos meios de comunicação social. Como consequência natural da publicidade, os doentes com cancro de todo o mundo perguntam-se se o Enhertu também lhes pode ser aplicável.
Como sempre, estamos aqui para nos distrairmos e analisarmos os dados disponíveis. Neste artigo, vamos rever tudo o que há para saber sobre Enhertu para o cancro do ovário.
Que tipo de cancro é tratado pelo Enhertu ?
Os doentes de todo o mundo têm-se perguntado se o Enhertu pode curar todos os cancros. Infelizmente, não é esse o caso. E não é o caso por design. Enhertu é uma terapia direccionada especificamente para:
- Tumores com uma expressão de HER-2. HER-2 é uma proteína que se encontra na superfície de diferentes tipos de células do organismo. Ajuda no crescimento normal das células. No entanto, em determinados cancros, pode tornar-se hiperactiva devido a alterações ou mutações genéticas. A sobreexpressão do HER2 afecta entre 2% e 66% dos casos de cancro do ovário 5.
- Tumores que se espalharam para outras partes do corpo e/ou são inoperáveis 4. Futuros ensaios clínicos podem envolver Enhertu em fases anteriores do tratamento do cancro 6. No entanto, atualmente não é esse o caso.
Qual é a eficácia do Enhertu para o cancro do ovário?
O ensaio de fase 2 DESTINY-PanTumor02, em curso, tem como objetivo testar a atividade de Enhertu em vários cancros sólidos HER2-positivos. Um deles é o cancro do ovário. Os resultados provisórios do ensaio foram partilhados em junho de 2023 e revelam-se promissores.
Para os doentes com cancro do ovário, os principais resultados preliminares do ensaio são:
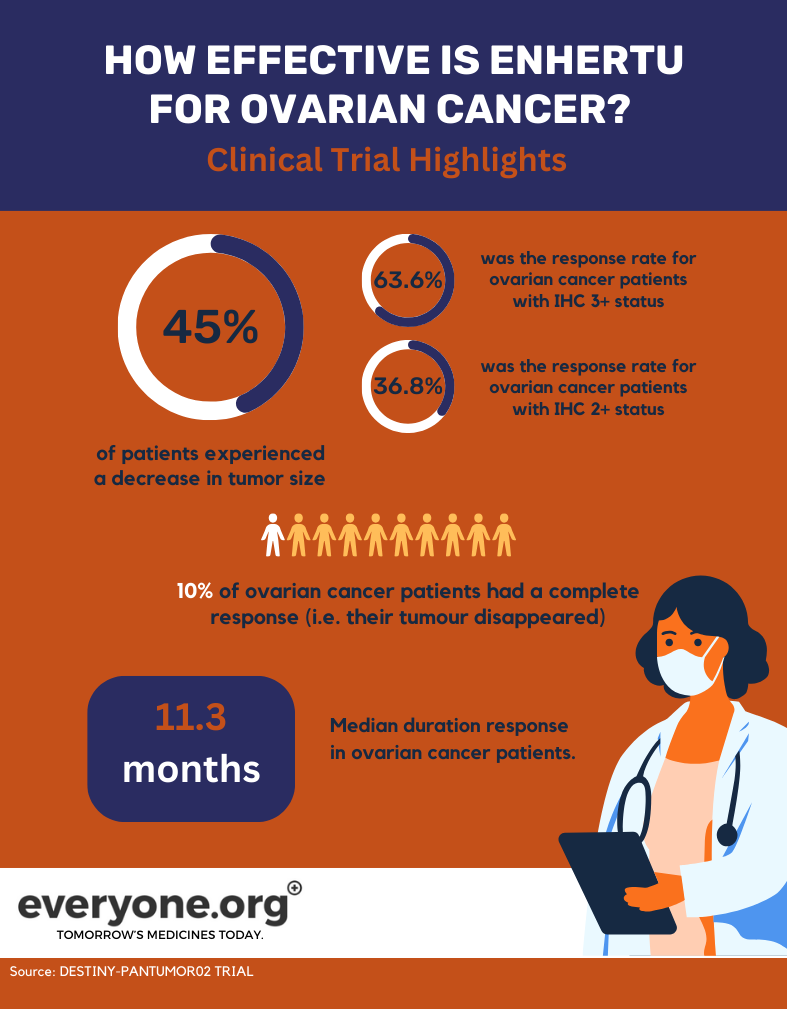
- A taxa de resposta global foi de 45,0%. Isto significa que 45% dos doentes tratados com Enhertu registaram uma redução dos seus tumores. Para os doentes com um estatuto HER2 de IHC 3+, a taxa de resposta global foi de 63,6%. Para os doentes com estatuto IHC 2+, a taxa de resposta foi de 36,8% 3.
- 10% das doentes com cancro do ovário tiveram uma resposta completa. Por outras palavras, o tumor desapareceu completamente 3.
- Ao fim de 12 meses, 45,8% das doentes com cancro do ovário com tumores que diminuíram de tamanho ou desapareceram ainda referiram sentir este benefício3.
- A duração média da resposta em doentes com cancro do ovário foi de 11,3 meses3.
Globalmente, estes resultados podem ser considerados encorajadores. A longa duração das respostas é um resultado particularmente notável, de acordo com o Dr. Meric-Bernstam (Presidente do Departamento de Terapêutica Investigacional do Cancro no MD Anderson Cancer Center dos EUA) 3.
Com base nos resultados destes estudos clínicos, a FDA dos EUA concedeu a Enhertu a primeira aprovação de sempre de um medicamento para ser utilizado em todos os cancros com expressão HER2.

Quando é que o Enhertu será aprovado para o cancro do ovário?
A partir de abril de 2024, Enhertu está aprovado para todos os cancros com expressão de HER2, incluindo o cancro do ovário.
O ensaio DESTINY-PanTumor02 está em curso, com resultados finais previstos para abril de 2027 7. No entanto, os resultados preliminares do estudo já eram suficientes para a recente aprovação do pan-tumor pela FDA.
Se residir fora dos EUA, o estado de aprovação do Enhertu para o cancro do ovário pode ser diferente.
O meu médico pode prescrever Enhertu para o cancro do ovário?
Atualmente, a melhor resposta é: talvez.
A partir de julho de 2024, Enhertu foi aprovado apenas nos EUA para o tratamento do cancro do ovário HER2-positivo. No entanto, mesmo noutros países, o seu médico tem autoridade para prescrever o medicamento para esta indicação de qualquer forma. Ele poderá fazê-lo com base nos resultados preliminares do ensaio clínico DESTINY-PanTumor02 e nas especificidades do seu caso.
Quando um médico prescreve um medicamento para o tratamento de uma doença para a qual não está aprovado localmente (ainda), chama-se a isso utilização não contemplada na rotulagem. Uma prescrição para uso off-label pode ser difícil de aviar em alguns países, dependendo dos regulamentos locais e da disponibilidade. No entanto, é sempre possível aviá-la utilizando o regulamento de importação de doentes nomeados.
O seu médico tomou a decisão de prescrever Enhertu para o tratamento do seu cancro do ovário? A nossa equipa em www.everyone.org pode ajudá-lo a aceder ao medicamento. Somos especializados no fornecimento e entrega de medicamentos prescritos não aprovados ou indisponíveis no país de um doente. Contacte-nos para o podermos ajudar.
Referências:
- Stewart, Judith. Enhertu (fam-trastuzumab deruxtecan-nxki) Histórico de aprovação da FDA. Drugs.com, 15 de agosto de 2022.
- Terapia inovadora. FDA, 4 de janeiro de 2018.
- Doherty, Kyle. Enhertu É promissor para cancros sólidos difíceis de tratar. Cure Today, 6 de junho de 2023.
- USPI-DB-04 CDX Atualização FINAL. Daiichi Sankyo, Acedido em 3 de outubro de 2023.
- Teplinsky, Eleonora, e Franco Muggia. EGFR and HER2: is there a role in ovarian cancer?, Translational Cancer Research, 13 de fevereiro de 2015.
- Liu, Angus. ASCO: Enhertu proporciona uma atividade pan-tumoral "muito convincente". Fierce Pharma, 5 de junho de 2023.
- A Phase 2 Study of T-DXd in Patients With Selected HER2 Expressing Tumors (DPT02), ClinicalTrials.gov, Acedido a 03 de outubro de 2023.