O Enhertu pode tratar o cancro colorrectal? Últimos resultados, prazos de aprovação e muito mais.
Última atualização: 15 de julho de 2024
Pode aceder legalmente a novos medicamentos, mesmo que estes não estejam aprovados no seu país.
Saiba comoDesde a sua primeira aprovação pela FDA em 2019, Enhertu tem ganho muita atenção no mundo da oncologia. Em 2023, Enhertu continua a sua impressionante trajetória com duas designações adicionais de avanço da FDA. Possui agora um total de sete 1.
Uma das mais recentes conquistas de Enhertu é a sua aprovação como tratamento de diagnóstico do cancro. Isto significa que pode agora ser aplicado a todos os doentes com tumores que expressam HER2, incluindo o tumor colorrectal. Para todos os doentes com cancro colorrectal, este é um marco importante. Ao mesmo tempo, coloca muitas questões.
Eis tudo o que precisa de saber sobre Enhertu para o cancro colorrectal.
O Enhertu tem aprovação da FDA para o cancro colorrectal?
Sim. Em abril de 2024, Enhertu foi aprovado para utilização em todos os tipos de cancro em que esteja presente uma expressão HER2. Isto também inclui o cancro colorrectal.
Para que tipos de cancro é aprovado o Enhertu ?
Enhertu é atualmente aprovado pela EMA na Europa para o tratamento de:
- Cancro da mama HER2-positivo metastático, que não pode ser removido cirurgicamente;
- Cancro da mama metastático HER2-low, que não pode ser removido por cirurgia;
- Cancro gástrico avançado HER2-positivo (cancro do estômago) ou cancro da junção gastro-esofágica 4.
Nos EUA, Enhertu está adicionalmente aprovado para o tratamento de:
- Cancro do pulmão de células não pequenas metastático com mutação HER2 5.
- todos os tumores sólidos com expressão de HER2.
Qual é a eficácia do Enhertu para o cancro colorrectal?
Uma vez que o Enhertu é uma terapia direccionada, só é aplicável a cancros com uma expressão de HER-2. Cerca de 3-5% de todos os cancros colorrectais enquadram-se nesta categoria 6.
Resultados dos ensaios clínicos
Em junho de 2023, foram publicados os resultados finais do ensaio DESTINY-CRC01. Este ensaio de fase 2 centrou-se na avaliação da eficácia e segurança de Enhertu em doentes com cancro colorrectal metastático com expressão de HER2. Os pacientes no ensaio tinham tumores que progrediram após pelo menos 2 rodadas anteriores de tratamento 7.
Os principais resultados deste ensaio para os doentes com cancro colorrectal foram
-
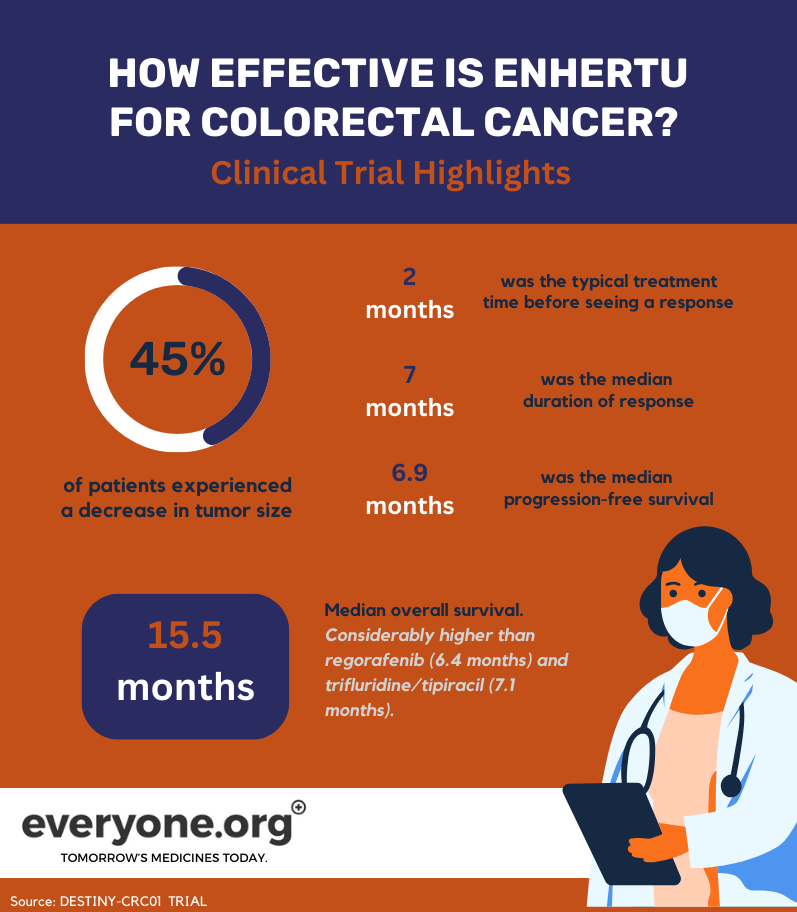
45,3% dos doentes tratados com Enhertu registaram uma redução parcial dos seus tumores;
-
A resposta ao tratamento foi normalmente observada cerca de 2 meses após o início do tratamento;
-
A duração média da resposta foi de 7 meses;
-
A mediana da sobrevivência sem progressão foi de 6,9 meses;
-
A sobrevivência global mediana foi de 15,5 meses. Este resultado excede significativamente o padrão de tratamento atual. Por exemplo, regorafenib e trifluridine/tipiracil são terapias comuns de terceira linha. Estes tratamentos têm uma sobrevivência global de 6,4 meses e 7,1 meses, respetivamente 7.
Um outro ensaio, denominado DESTINY-CTC02, está a estudar o Enhertu em doentes com cancro colorrectal. Este ensaio ainda está a decorrer, mas os seus resultados preliminares estão em conformidade com os resultados do ensaio DESTINY-CTC01 10.

Quão seguro é o Enhertu para o cancro colorrectal?
Em termos de segurança, estes são os principais resultados do ensaio DESTINY-CRC01:
-
Cada doente teve um efeito secundário do tratamento. Os efeitos secundários mais comuns foram problemas de estômago e de sangue.
-
Ocorreram efeitos adversos graves em 37,7% dos doentes. Os efeitos secundários graves mais comuns foram contagens baixas de neutrófilos (22,1%) e anemia (14%) 7.
-
Um efeito secundário denominado doença pulmonar intersticial (DPI) foi associado à descontinuação do medicamento e foi observado em 7% dos doentes.
-
Foram registadas 3 mortes relacionadas com o medicamento, todas elas associadas a doença pulmonar intersticial.
O que é que isto significa?
Enhertunão podem ser diretamente comparados entre diferentes grupos de doentes. No entanto, para o ajudar a colocar as coisas em contexto, eis um resumo dos resultados de segurança de Enhertu em vários tipos de tumores. Incluindo tumores para os quais o Enhertu está aprovado:
-
A DPI ocorreu em 12% dos pacientes do estudo, com desfecho fatal em 1,5% dos casos;
-
A diminuição da contagem de neutrófilos ocorreu em 34,6% dos doentes do ensaio;
-
Ocorreu anemia em 34-43% dos doentes do ensaio (dependendo da dosagem do medicamento) 8.
Tendo isto em conta, o perfil de segurança de Enhertu para o cancro colorrectal é semelhante ao seu perfil para outros cancros aprovados.
Quando é que o Enhertu será aprovado para o cancro colorrectal?
Enhertu já está aprovado pela FDA para o cancro colorrectal HER2-positivo - uma indicação que se enquadra na mais recente aprovação da FDA de Enhertu.
No entanto, esta última aprovação é apenas um facto nos EUA. O que significa isto para os doentes com cancro colorrectal noutros países? Que papel poderá desempenhar o Enhertu no seu tratamento do CCR?
O meu médico pode prescrever Enhertu para o cancro colorrectal?
A resposta curta é sim.
Enhertu já está aprovado pela FDA para o tratamento do cancro colorrectal HER2-positivo. Mesmo que se encontre noutro país, o seu médico tem autoridade para prescrever o medicamento para esta indicação. Ele poderá fazê-lo com base nos resultados finais do ensaio DESTINY-CRC01 ou nos resultados preliminares do ensaio DESTINY-CRC02, e nas especificidades do seu caso.
Se um médico lhe der um medicamento para uma doença para a qual não está aprovado localmente, trata-se de uma utilização não contemplada na rotulagem. Em alguns países, aviar uma receita de uso não autorizado pode ser um desafio devido aos regulamentos e à disponibilidade locais. No entanto, é sempre possível aviá-la utilizando o regulamento de importação de doentes nomeados.
O seu médico tomou a decisão de prescrever Enhertu para o tratamento do seu cancro colorrectal? A nossa equipa em www.everyone.org pode ajudá-lo a aceder ao medicamento. Somos especializados no fornecimento e entrega de medicamentos prescritos não aprovados ou indisponíveis no país do doente. Contacte-nos, para que o possamos ajudar.
Referências:
- Barrie, Robert. Enhertu ganha duas designações de terapia inovadora da FDA. Pharmaceutical Technology, 31 de agosto de 2023.
- A FDA concede designações de terapia inovadora ao Trastuzumab Deruxtecan para tumores sólidos HER2+, incluindo mCRC. OncLive, 31 de agosto de 2023.
- Terapia inovadora. FDA, 4 de janeiro de 2018.
- Enhertu |Agência Europeia de Medicamentos. Agência Europeia de Medicamentos, Acedido em 30 de outubro de 2023.
- Stewart, Judith. Enhertu (fam-trastuzumab deruxtecan-nxki) Histórico de aprovação da FDA. Drugs.com, 15 de agosto de 2022.
- Biomarcador HER2 no cancro do cólon. Know Your Biomarker, 24 de maio de 2023.
- Resultados finais do estudo DESTINY-CRC01 que investiga o trastuzumab deruxtecan em doentes com cancro colorrectal metastático com expressão de HER2. Nature Communications, Acedido em 30 de outubro de 2023.
- Enhertu, DCI-trastuzumab deruxtecan. Agência Europeia de Medicamentos , Acedido em 30 de outubro de 2023.
- Trastuzumab Deruxtecan em Participantes com Cancro Colorrectal Avançado ou Metastático com Expressão HER2 (DESTINY-CRC02). ClinicalTrials.gov, Acedido em 30 de outubro de 2023.
- Trastuzumab deruxtecan (T-DXd) em doentes (pts) com cancro colorrectal metastático (mCRC) com expressão/amplificação de HER2 (HER2+): Primary results from the multicenter, randomized, phase 2 DESTINY-CRC02 study. Journal of Clinical Oncology, Acedido em 30 de outubro de 2023.